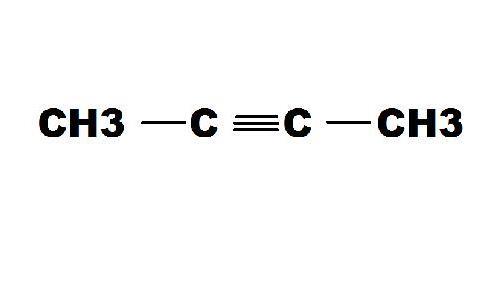Алкины – це насичені вуглеводні, які мають у своїй будові потрійну зв’язок, крім одинарною. Загальна формула ідентична з формулою алкадиенов – c n h 2n-2. Потрійний зв’язок має фундаментальне значення в характеристиці даного класу речовин, його ізомерії і будову.
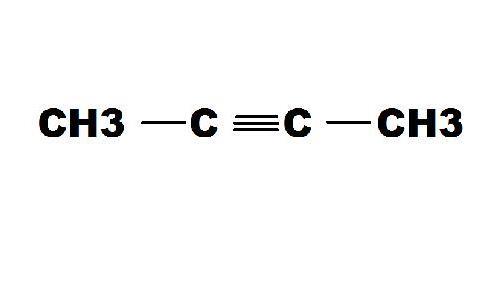
Загальна характеристика потрійний зв’язку
Атоми вуглецю, що утворюють потрійну зв’язок, мають sp-гібридизацію. Виходячи з методу локалізованих електронних пар, цей зв’язок, як відомо, утворюється перекриванням двох р-орбіталі, що знаходяться в перпендикулярному положенні і однієї s-орбіталі, що з’єднує атоми. Таким чином, накладання гібридної орбіталі забезпечує утворення однієї сигма-зв’язку, а двох негибридных – утворення двох пі-зв’язків. Варто відзначити, що потрійний зв’язок коротше подвійний, а енергія, що виділяється при її розриві, набагато більше. Тому і потрійний зв’язок набагато міцніше.
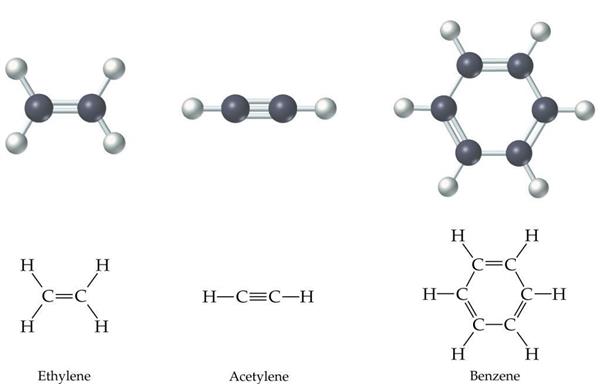
Отже, вище розглянули будову алкіной, ізомерія і номенклатура будуть вивчені в наступних пунктах.