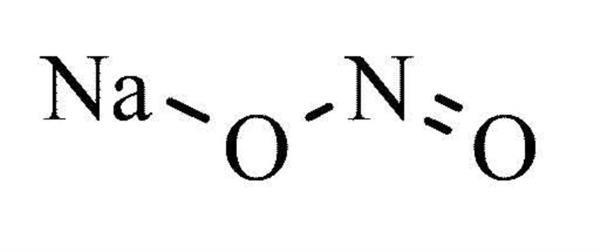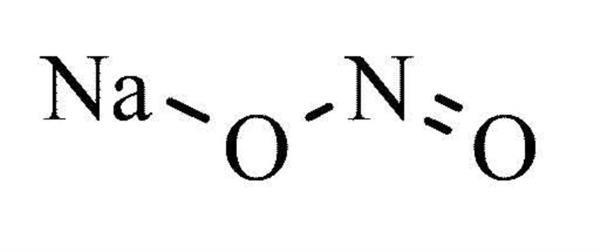Нітрит-іон — це іон, що складається з одного атома азоту і двох атомів кисню. Азот в цьому іоні має заряд +3, отже заряд всього іона -1. Частка одновалентна. Формула нітрит-іона NO2-. Аніон має нелінійну конфігурацію. Сполуки, що містять цю частку, називаються нітритами, наприклад нітриту натрію NaNO2, нітрит срібла — AgNO2.
Фізичні і хімічні властивості
Нітрити лужних, лужноземельних металів та амонію являють собою безбарвні чи злегка жовтуваті кристалічні речовини. Нітрити калію, натрію, барію у воді добре розчиняються, нітрити срібла, ртуті, міді – погано. З підвищенням температури розчинність підвищується. Практично всі нітрити погано розчиняються у ефірах, спиртах і малополярних розчинниках.
Таблиця. Фізичні характеристики деяких нітритів.
| Характеристика | Нітрит калію | Нітрит срібла | Нітрит кальцію | Нітрит барію |
|
Тпл, °З |
440 |
120 (з разлож.) |
220 (з разлож.) |
277 |
|
∆Н0обр, кДж/моль |
– 380,0 | – 40,0 | -766,0 | – 785,5 |
| S0298, Дж/(моль*К) | 117,2 | 128,0 | 175,0 | 183,0 |
| Розчин-ть у воді, г в 100 г |
306,7 (200С) |
0,41 (250С) |
84,5 (180С) |
67,5 (200С) |
Нітрити малостійкі до нагрівання: плавляться без розкладання тільки нітрити лужних металів. У результаті розкладання виділяються газоподібні продукти — O2 , NO, N2, NO2, і тверді речовини — оксид металу або сам метал. Наприклад, розкладання нітриту срібла(йде вже при 40 °С) супроводжується виділенням елементного срібла і оксиду азоту (II):
2AgNO2 = Agno 3 + Ag + NO↑
Оскільки розкладання йде з виділенням великої кількості газів, реакція може йти з вибухом, наприклад, у разі нітриту амонію.