Біфторид амонію — токсична неорганічне з’єднання промислового виробництва, що використовується в скляній, нафтової й металургійної сферах. Речовина часто застосовується в якості заміни плавикової кислоти або фтористого водню.
Загальний опис та фізичні властивості
Біфторид амонію найчастіше має твердий агрегатний стан і представлено у вигляді кристалів. Останні характеризуються високою розчинністю у воді, але нульовий — в ацетоні і спирті. Кристали мають орторомбическую сингонию з дискретною групою рухів Р man. Речовина розкладається при температурі понад 238 °С.

Даний біфторид не має пожежонебезпечними та вибухонебезпечними властивостями.
Структура і хімічна формула
Речовина має декілька синонімічних найменувань, таких як біфторид фториду амонію, амоній фтористий кислий, гидрофторид амонію і т. д. Це з’єднання має хімічну формулу NH4(HF2).
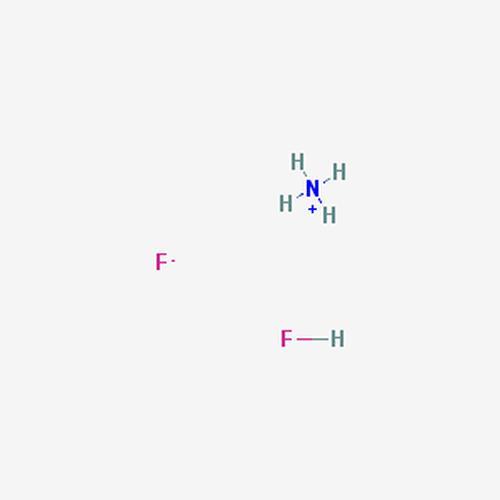
В хімічний склад речовини входять:
- катіон амонію (NH4+);
- біфторид або водень діфторіда;
- аніон (HF2-).
Примітною особливістю цього з’єднання є присутність найсильнішою водневої зв’язку з довжиною 114 мкм. Вона з’єднує фтор і водень в центросимметричном триатомном бифторидном анионе. Енергія зв’язку перевищує 155 кДж/моль-1.
В кристалічній формі речовини кожен катіон амонію оточують чотири фторідних центру, утворюючи тетраедр.
Форма виробництва
Біфторид амонію проводиться в двох формах:
- твердої (білі кристали);
- у вигляді розчину.

Розчин являє собою прозору рідину із запахом. Концентрація вихідної речовини в такій суміші становить від 28 до 30 %.
Використання речовини
Біфторид амонію має дуже широкий спектр застосування. Зокрема його використовують для:
- обробки скла;
- анодування алюмінію;
- в якості замінника більш токсичною і агресивної плавикової кислоти, що покращує екологічність і знижує витрати скляної обробки;
- очищення металевих поверхонь;
- дезинфікування теплових трубопроводів, виробів зі шкіри та дерева;
- лиття марганцю (у якості флюсу);
- видалення піску з нафтових свердловин;
- усунення іржі в котлах і трубах;
- промивання нафтових проводів.
Заміна плавикової кислоти на гидрофторид амонію застосовується не тільки в скляній обробці, але і в бурінні свердловин.
Характеристика токсичності
Клас небезпеки бифторида амонію — АДР 8. Це достатньо токсична для організму людини речовина із сильним корозійним дією. При контакті з шкірою це з’єднання викликає роздратування, а при тривалому впливі — опіки. Попадання бифторида амонію в очі може викликати пошкодження зорового органу.
Вдихання кисню в сукупності з цією речовиною викликає такі симптоми:
- подразнення слизових носоглотки і дихальних шляхів;
- носові кровотечі;
- кашель;
- хрипи;
- задишка;
- нудота і блювання.
Взаємодія бифторида амонію з водою призводить до утворення дуже небезпечною фтористоводневої кислоти, що посилює травмує ефект цього з’єднання при попаданні на вологу шкіру. У разі тривалого і інтенсивного впливу речовини на організм його вплив призводить до отруєння фтором, болі в шлунку, появи слабкості, судом і навіть смерті.
Регулярний контакт людини з бифторидом амонію призводить до розвитку патологічного стану, що називається флюорозом, при якому відбувається відкладення фторидів в кістках і зубах.
Екологічність
Для навколишнього середовища це речовина менш небезпечно, ніж для людини при безпосередньому контакті. Біфторид амонію має дуже важливим екологічним якістю — швидким розкладанням (протягом кількох днів), що виключає можливість її накопичення.
Тим не менш у вологому середовищі це речовина розпадається на фтороводородную кислоту і аміак, які токсичні для живих організмів.

