Аліфатичні амінокислоти – похідні карбонових кислот – широко поширені в природі. Вони відіграють важливу роль у багатьох життєво важливих процесах. На їх основі виготовляють деякі види лікарських засобів.
Аліфатична амінокислота – що це?
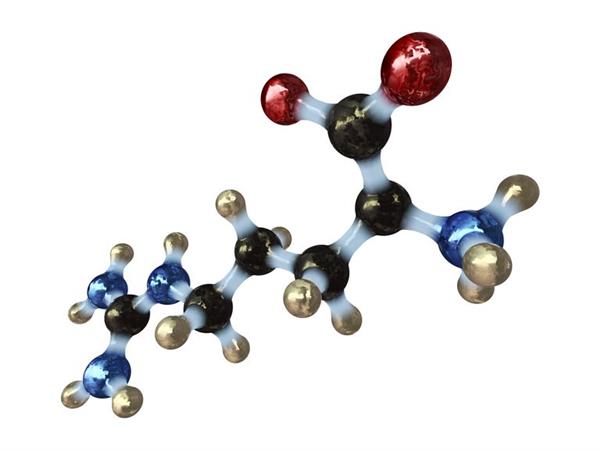
Амінокислоти виконують важливі функції в організмі людини та інших тварин, так як є нейромедиаторами і «цеглинками» для побудови білків. Також вони потрібні для правильного обміну речовин.
Аліфатичні амінокислоти – це різновид амінокарбонових амінокислот, у яких аміно – та карбоксильна групи пов’язані з аліфатичних атомом вуглецю. Термін «аліфатичний» передбачає лінійні або розгалужені ланцюги з атомів даного елемента.
Основна маса амінокислот, які були виділені з живих організмів, що відносяться саме до аліфатичних. У хімії використовують, в основному, обігові назви цих речовин по вихідним білків, з яких вони були отримані, так як за систематичною номенклатурою у них занадто громіздкі найменування.
Типи сполук за будовою
Аліфатичні амінокислоти, в залежності від положення аміно – і карбоксильних груп, підрозділяють на наступні види:
-
Альфа-ізомери. До них відноситься основна маса природних сполук, які знаходяться в рослинах, мікроорганізмах, тварин. Їх знаходять також в метеоритах, причому структура цих речовин така ж, як і у земних живих істот.
-
Бетта-амінокислоти. Прикладом є β-аланін, який служить частиною коферменту А Останній приймає участь у синтезі та окисленні жирних кислот.
-
Гамма-ізомери. Один з яскравих представників цієї групи – ɣ-аміномасляна кислота (ГАМК), найважливіший нейромедіатор нервової системи, що відповідає за гальмування нервових процесів, ослаблення і пригнічення збудження.
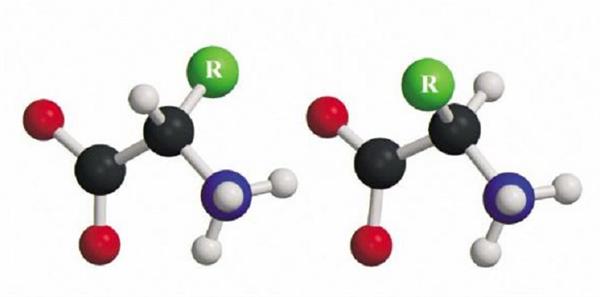
Всі амінокислоти альфа-типу, крім гліцину, мають асиметричну структуру, існують у вигляді двох дзеркальних, не поєднуваних у просторі відбиттів (L – і D-амінокислоти) і мають природної оптичної активністю. Найважливішими L-амінокислотами є гліцин, аланін, серин, цистеїн, аспарагінова кислота, тирозин, лейцин, глутамін, ізолейцин, аргінін, лізин, пролін.
Приклади аліфатичних амінокислот наведено на малюнку нижче.

Види речовин за іншими критеріями
Існує також класифікація за характером участі аліфатичних амінокислот у синтезі білка.
-
Протеиногенные з’єднання з L-ряду, які приєднуються до складу білків у рибосомах під контролем РНК. Їх послідовність кодується генетично. Таких амінокислот всього двадцять.
-
Непротеиногенные (некодируемые), що не входять в склад білків, але виконують важливі функції (в основному, участь в обмінних процесах). Деякі з них є токсинами і отруйні для людини.
За кислотно-основними властивостями аліфатичні амінокислоти поділяють на 3 типи:
-
кислі (аспарагінова і глутамінова кислоти);
-
нейтральні, містять одне і те ж число основних і кислотних груп;
-
основні (гістидин, аргінін, лізин та інші).
Фізико-хімічні характеристики

Для аліфатичних амінокислот характерні наступні властивості:
-
структура у вигляді біполярних іонів в кристалічному стані;
-
висока температура плавлення (у α-амінокислот її немає чіткого значення);
-
хороша розчинність у воді і водних розчинах лугів, кислот;
-
амфотерність;
-
основні властивості в кислому середовищі і навпаки;
-
якщо pH середовища більше, ніж изоэлектрическая точка, то аліфатичні амінокислоти утворюють солі з лугами, які добре розчиняються у воді.
З сумішей цих речовин за їх натрієвими чи калієвими солями роблять буферні розчини, застосовувані для хімічного аналізу.
Синтез
В лабораторних умовах виробництво даних сполук являє собою складну задачу, так як вони є оптично активними, і в природних умовах їх вироблення відбувається з участю ферментів. Тому хімічним шляхом отримують тільки рацемические амінокислоти, що представляють собою суміш оптичних ізомерів.
В якості вихідної речовини застосовують α-галоидкарбоновые кислоти, які при реагуванні з аміаком дають аліфатичні амінокислоти. Існують і інші способи отримання – з кетокислот та їх похідних в процесі відновного амінірованіе, малонового ефіру, аминоуксусной кислоти (гліцину). Для синтезу амінокислот в промисловому масштабі використовують мікробіологічні технології. За допомогою генної інженерії ці речовини виділяють з білкових молекул, що виробляються спеціально культивованими мікроорганізмами.
Роль у природі

Тільки в рослинах і мікроорганізмах виявлено понад 200 аліфатичних амінокислот, а всього їх налічується на сьогоднішній день понад п’ятисот. Вони входять до складу антибактеріальних речовин (наприклад, пеніциліну), які виробляють мікроорганізми, а також формують клітинні стінки більшості бактерій.
В організмі тварин ці речовини виконують наступні основні функції:
-
синтез білків, ферментів, гормонів, коензимів та інших важливих органічних сполук;
-
утворення біологічно активних амінів (дофамін, норадреналін, адреналін, серотонін та інших);
-
участь у передачі нервових імпульсів і в метаболічних процесах.
У клітинах головного мозку людини відбувається активний обмін речовин з участю амінокислот, концентрація яких перевищує в 7 разів таку в плазмі крові.
Застосування в медицині
Використання цих сполук в лікувальних цілях засновано на їх властивості брати участь в обміні азотистих елементів та синтезі біологічно активних речовин. Існує безліч препаратів, де містяться аліфатичні амінокислоти. Нижче перераховані деякі з них і їх призначення в терапевтичній практиці.
-
Глутамінова кислота – патології ЦНС, епілепсія, психози, затримка психічного розвитку у дітей, ДЦП, хворобу Дауна.
-
Метіонін – токсичні ураження печінки (цироз, отруєння миш’яком, хлороформом та іншими токсинами), а також захворювання цього органу при хронічному алкоголізмі, цукровому діабеті.
-
Аміналон – нейротропну засіб.
-
Цистеїн – при катаракті.
-
Ацетилцистеїн – при захворюваннях органів дихання в якості муколитика.

