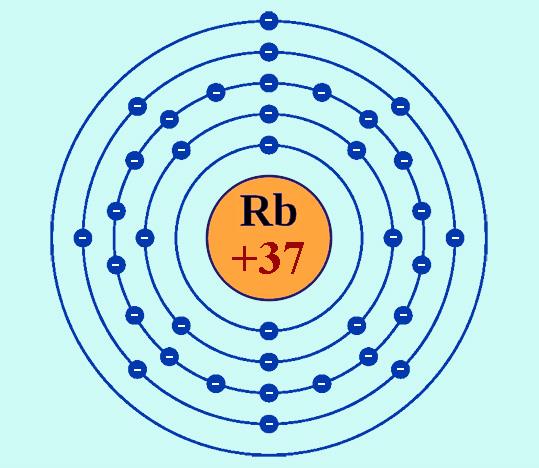
Основні хімічні властивості
Як було зазначено вище, у ряді хімічних елементів рубідій (як натрій, калій, літій, цезій і францій) належить до лужних металів. Особливість електронної конфігурації їх атомів, що визначає хімічні властивості – це наявність тільки одного електрона на зовнішньому енергетичному рівні. Цей електрон легко залишає атом, а іон металу при цьому набуває енергетично вигідну електронну конфігурацію, який стояв перед ним в таблиці Менделєєва інертного елемента. Для рубідію це – конфігурація криптону.
Таким чином, рубідій, як і інші лужні метали, має яскраво виражені відновлювальні властивості та ступінь окислення +1. Лужні властивості сильніше проявляються зі збільшенням атомної ваги, оскільки при цьому зростає і радіус атома, і, відповідно, послаблюється зв’язок зовнішнього електрона з ядром, що зумовлює підвищення хімічної активності. Тому рубідій активніше літію, натрію та калію, а цезій, у свою чергу, активніше рубідію.
Підсумовуючи все вищесказане про рубидии, розбір елемента можна зробити, як на ілюстрації, представленої нижче.