Фізичні характеристики
Для хлористого бензила характерні наступні властивості:
- легка займистість;
- щільність (при 25 °C) – 1100 кг/м3;
- молярна маса – 126,58 г/моль;
- температура плавлення – До 234,2;
- температура кипіння – 452,5 До;
- температура спалаху – 426,2 До;
- межа вибуховості пари – 1,1% (за об’ємом).
У речовини є схильність до самоконденсации. Її усувають шляхом додавання вуглеводнів, смол і фенолів.
За зовнішнім виглядом це з’єднання являє собою безбарвну рідину.
Хлористий бензил: отримання
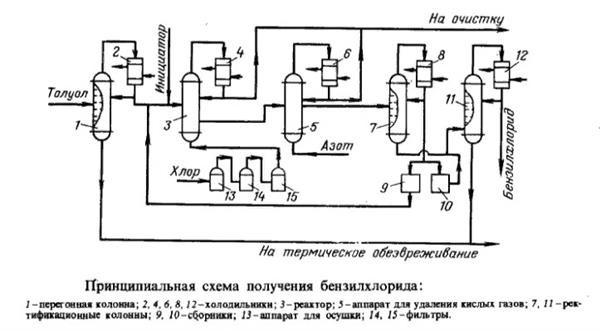
Основним промисловим способом синтезу даної речовини є хлорування толуолу при температурі 90-100 °C. Принципова технологічна схема цього процесу зображена на малюнку нижче.
Хімізм реакції протікає наступним чином:
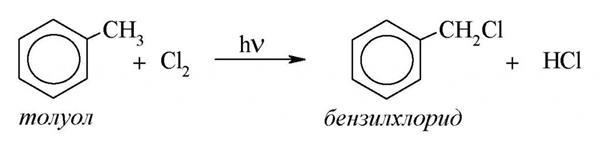
Технологія складається з 3 основних стадій:
- дистиляція толуолу;
- його хлорування;
- поділ багатокомпонентного продукту реакції.
В якості ініціаторів, які запускають ланцюгові радикальні процеси, застосовують ультрафіолетове опромінення або C₈H₁₂N₄ (динитрил азобисизомасляной кислоти). В кінцевому продукті масова частка хлористого бензила становить не менше 98%. Побічними речовинами в суміші є поліхлориди (бензилиденхлорид), хлортолуол і толуол.
Утворення сполук першого типу обумовлено електрофільним заміщенням атома водню ароматичного ядра на атом хлору, каталізатором якого є хлористе залізо. Цьому також сприяє зростання концентрації бензилхлорида в реакторі. З цієї причини процес хлорування проводять не до кінця. Кількість вихідного толуолу в залишку становить до 50%. У цьому випадку зміст полихлоридов не перевищує 5% від маси хлористого бензила.
На процес хлорування толуолу надає великий вплив також чистота реагентів. Так, при наявності домішок заліза відбувається хлорування толуолу в ядро, а пари води призводять до швидкого руйнування металу технологічного обладнання. Найбільш підходящими матеріалами для реакторів є срібло і нікель. Одним із перспективних способів зниження утворення побічних продуктів служить використання амінів (диметиламин, діетиламін, діетаноламін), які здатні зв’язувати хлорне залізо у неактивні комплекси.
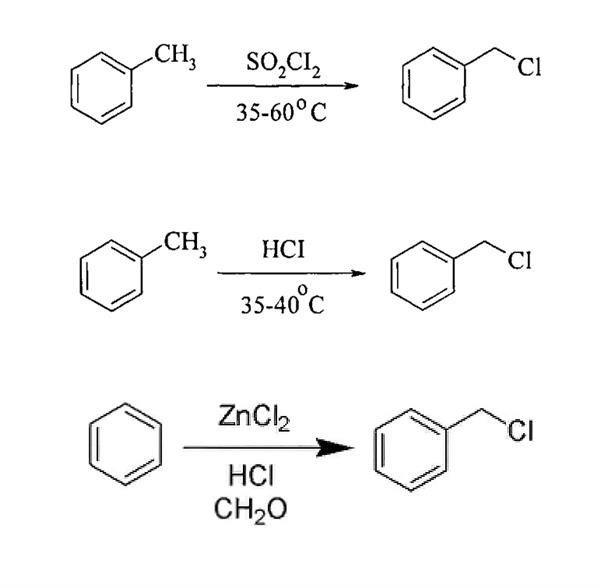
Застосовуються й інші способи одержання цієї сполуки, вказані на малюнку нижче.