Застосування
Калій відіграє важливу біологічну роль в організмі людини і розвитку рослин. Крім того, він широко використовується в повсякденному житті. Так, в комплексі з азотом і фосфором він є незамінним добривом для культурних рослин, що дозволяє підвищити їх врожайність, вегетативну масу і стійкість до шкідників.

Сплав металу з натрієм використовується для передачі теплової енергії в замкнутих системах, а якщо до цього з’єднанню додати цезій, вийде склад з рекордно низькою температурою плавлення (мінус 78 градусів Цельсія).
Для того щоб використовувати всі ці корисні і важливі сполуки, потрібно знати реакції отримання калію з його сполук.
Одержання металу
Неорганічне з’єднання білого кольору, гідрид калію, що утворюється з розплавленого металу, але воно нестабільно і при температурі 400 градусів Цельсія у вакуумі розпадається на складові по наступній реакції:
- 2КН = 2К + Н2.
Гідроксид калію утворюється з відповідного хлориду. Він широко застосовується у виробництві рідких мил і для отримання калію і його сполук. Для цього потрібно провести електроліз, тобто пропустити через розчин струм. В результаті на аноді утворюється кисень, а на катоді калій:
- 4КОН = 4К + О2 + 2Н2О.
З хлориду можна отримувати не тільки гідроксид, але і метал у чистому вигляді. Для цього також потрібно реакція електролізу розчину:
- 2KCl = 2К + Cl2.
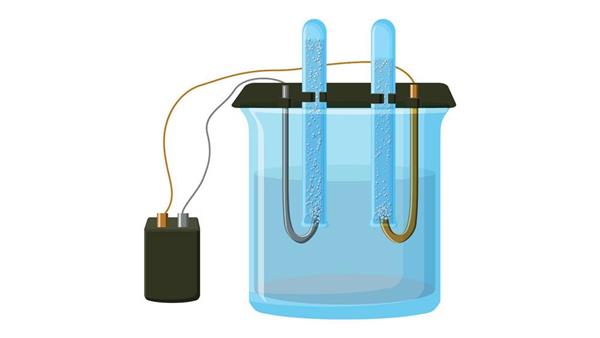
На відміну від попереднього способу отримання калію, в цьому можна використовувати вихідна речовина не тільки в рідкому стані, але і у вигляді розплаву, але в цьому випадку відбуваються два паралельні реакції:
- 2KCl + 2Н2О = Н2 + Cl2 + 2КОН;
- 2KCl = 2К + Cl2.
Катод, на якому буде утворюватися калій, повинен бути ртутним.

