Сульфування бензолу, а також інших ароматичних вуглеводнів – одна з найважливіших реакцій в органічній хімії, так як її продукти знаходять широке промислове застосування. Для отримання сульфокислот бензол обробляють сірчаною кислотою, олеумом. Сульфування може також проводитися ступінчасто для створення декількох функціональних груп.
Принцип сульфування
Сульфування бензолу являє собою введення сульфогрупи SO3H – заміщення нею атома водню в органічному поєднанні. В результаті отримані речовини набувають кислотні властивості і стають розчинними у воді. В подальшому, шляхом відщеплення сульфогруп, можна синтезувати інші сполуки – аминобензол (анілін), галогенобензол, нітробензол, гидроксибензол (фенол).
Цьому процесу піддають не тільки самі вуглеводні, але і їх похідні. Гомологічні з’єднання бензолу (толуол і ксилол) сульфируются легше, а найбільш активно дана реакція проходить з аніліном та фенолом.
Реакція сульфування бензолу, поряд з нитрированием, є однією з найбільш характерних для ароматичних вуглеводнів. Заміщення водню у таких речовин протікає набагато легше, ніж у аліфатичних органічних сполук.
Сульфирующие агенти
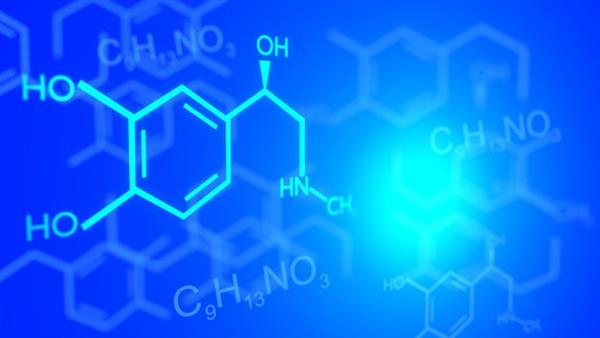
Як сульфирующих агентів можуть застосовуватися наступні речовини:
- сірчана кислота H2SO4 в різної концентрації;
- олеум (димляча сірчана кислота);
- хлорсульфоновая кислота – HSO₃Cl;
- сірчаний ангідрид;
- купоросное масло (H2SO4 в концентрації 93% і більш);
- моногідрат сірчаної кислоти;
- сульфурилхлорид SO₂Cl₂;
- лужні солі сірчистої кислоти;
- полисульфаты;
- кислі солі сірчаної кислоти.
Найбільш часто в механізмі сульфування бензолу застосовується олеум – розчин SO3 в стовідсотковою сірчаної кислоті. Сорти олеуму підбираються такі, у яких концентрація триоксиду сірки складає близько 65%, так як дані склади залишаються рідкими при звичайних умовах. При використанні цієї речовини механізм реакції сульфування бензолу відбувається з високою швидкістю.
Процес сульфування: опис
Реакція бензолу з олеумом відбувається так:
C6H6 + H2SO4 —> C6H5-SO3H + H2O.
Структурно порядок реакції сульфування бензолу виглядає наступним чином:
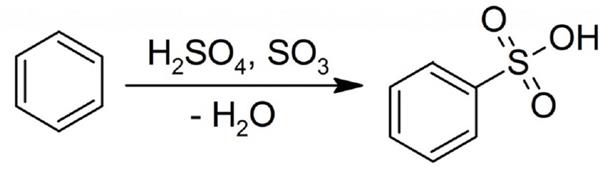
Цільовим продуктом є сульфокислоти. При обробці 92-94% сірчаною кислотою їх вихід становить 90-96%.
Сульфування при 3-кратному надлишку концентрованої сірчаної кислоти протікає по схемі:
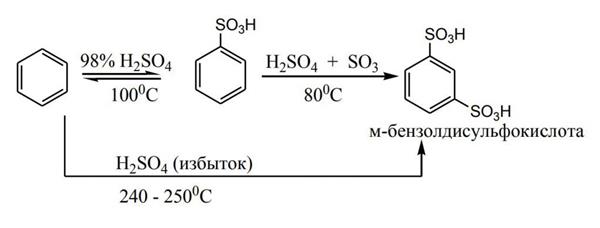
Так як процес йде повільно (хоча при цьому виділяється тепло), то потрібно нагрівання.
До недоліків сульфування бензолу сірчаною кислотою відносять:
- невелика концентрація електрофілов;
- швидке падіння швидкості реакції при розведенні кислоти водою;
- агресивність реакційної середовища;
- необхідність застосування нейтралізуючих реагентів, велика кількість відходів (екологічний аспект).
Властивості продукту
Хімічні властивості бензолу при сульфируванні характеризуються наступними особливостями:
- безбарвна або світло-жовте легкоплавкое кристалічна речовина з різким запахом;
- хороша розчинність у воді, практично повна дисоціація;
- висока поглинаюча здатність щодо парів води, на повітрі кристали розпливаються;
- яскраво виражений кислотний характер;
- з’єднання розкладається водою з виділенням токсичних газів;
- пари важчі за повітря;
- константа кислотності – у межах 5,0-8,0.
Одне з найбільш важливих властивостей сульфокислот – їх здатність обмінювати сульфогруппу на інші функціональні групи, безпосереднє введення яких в структуру ароматичних вуглеводнів є скрутним.
Введення декількох сульфогруп

Заміщення двох або трьох атомів водню проводиться поступово, шляхом поетапного зміни наступних параметрів:
- сульфирующий агент;
- концентрація або кількість цієї речовини;
- температура.
Отримання мета-бензолдисульфокислоты проводиться в 2 стадії:
- Сульфування C6H6 концентрованою кислотою H2SO4, в результаті чого утворюється моносульфокислота.
- Обробка продукту попередньої реакції надлишком 20% олеуму при температурі 100оС (або 60% при 60-80о С). Так як первинне введення сульфогрупи значно уповільнює подальше сульфування (приблизно в 10 000 разів), то друга реакція проводиться в більш жорстких умовах.
Подальше сульфування до 3 – і 5-бензолсульфокислоты можливо тільки при впливі олеумом в 60% концентрації при температурі 250оС в присутності каталізатора – сульфату ртуті.
У звичайних умовах реакція сульфування є оборотною, але якщо використовується олеум з високим вмістом ангідриду, то процес стає незворотнім. Те ж спостерігається при обробці бензолу хлорсульфонової кислоти.
Вплив температури
Підвищення температури при сульфируванні бензолу не тільки збільшує швидкість перебігу реакції, але і призводить до утворення побічних продуктів: полисульфокислот, сульфонов, оксидів. При нагріванні вище 160 °С відзначається поява дисульфокислот.
Тому кожна реакція повинна проводитися при певній температурі. Від неї залежить місце приєднання групи SO3H (регіоселективність) в ароматичних вуглеводнях.
Сульфування «в парах»
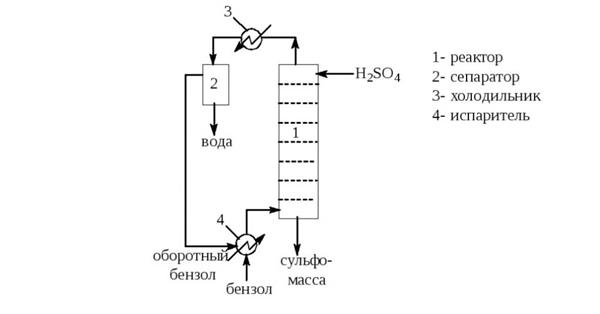
У виробничих умовах одним з найбільш економічних методів отримання бензолсульфокислоты є проведення реакції в «парах». Ця технологія дозволяє скоротити потребу H2SO4 майже в 2 рази, в порівнянні з процесом, при якому використовується рідка фаза цієї речовини. До недоліків реакції відноситься зниження швидкості сульфування.
Усунення недоліків, пов’язаних із застосуванням H2SO4 в рідкому стані, можливо шляхом видалення води з реакційної маси або застосуванням олеуму (підвищенням концентрації SO3).
Технологія сульфування бензолу в цьому випадку протікає наступним чином:
- Бензол з ємності подають в трубне обв’язування випарника за допомогою насоса. У цьому пристрої речовина нагрівається парою, проходить по трубах зовнішнім. Потім пари доводять до t=150 °С.
- Бензол в пароподібному стані в надлишку подають у реактор, де він проходить через шар концентрованої сірчаної кислоти при температурі 150 °С.
- У холодильнику C6H6 і H2O конденсуються і охолоджуються до температури 30 °С.
- В сепараторі відбувається розшарування суміші, а оборотний бензол повертають на сульфування.
Залишки бензолу в сульфомассе видаляють за допомогою отдувки повітрям. Потім суміш надходить на нейтралізацію в апарат, облицьований усередині кислототривкої плиткою. Ця реакція проводиться за участю водного розчину Na₂SO₃. Після обробки масу направляють у колону для усунення діоксиду сірки. Отриманий продукт використовують для отримання фенолу з допомогою лужного плавлення (в даний час цей процес втратив промислове значення, фенол синтезують з ізопропілбензолу) або упарюють до сухого залишку бензолсульфоната натрію.
Інші способи
Застосовують і інші методики сульфування бензолу:
- Рідкий вуглеводень пропускають протитечією крізь шар H2SO4. Отриманий продукт розчиняють спочатку в бензолі, а потім вимивають водою.
- Сульфування олеумом слабкої концентрації при підвищеній температурі 190-250 °С і тиску 1-3 МПа. Поява побічних продуктів пригнічується шляхом введення бензолсульфоната натрію.
Виділення сульфокислот
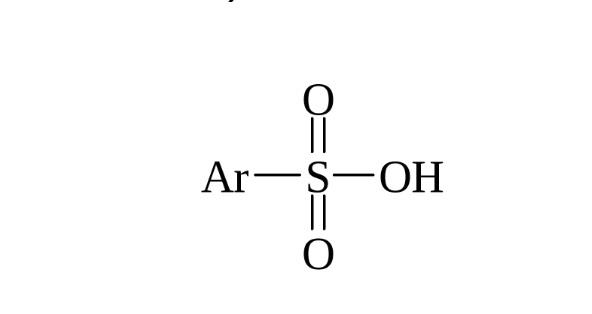
Так як продукти реакції добре розчинні, їх виділення виробляють у вигляді солей. Для цього в сульфомассу, при постійному помішуванні, вводять нейтралізують агенти, в якості яких застосовують такі речовини:
- сульфіт натрію;
- крейда;
- технічна сода;
- вапно.
Виділення вільних сульфокислот виробляють при реакції з іонообмінних смолах або підкисленням хлороводнем.

