Що таке нітробензол? Це органічна сполука, яка являє собою ароматичне ядро і приєднану до нього нітрогрупу. За зовнішнім виглядом, залежно від температури, — це яскраво-жовті кристали або масляниста рідина. Має мигдалевих запах. Токсичний.
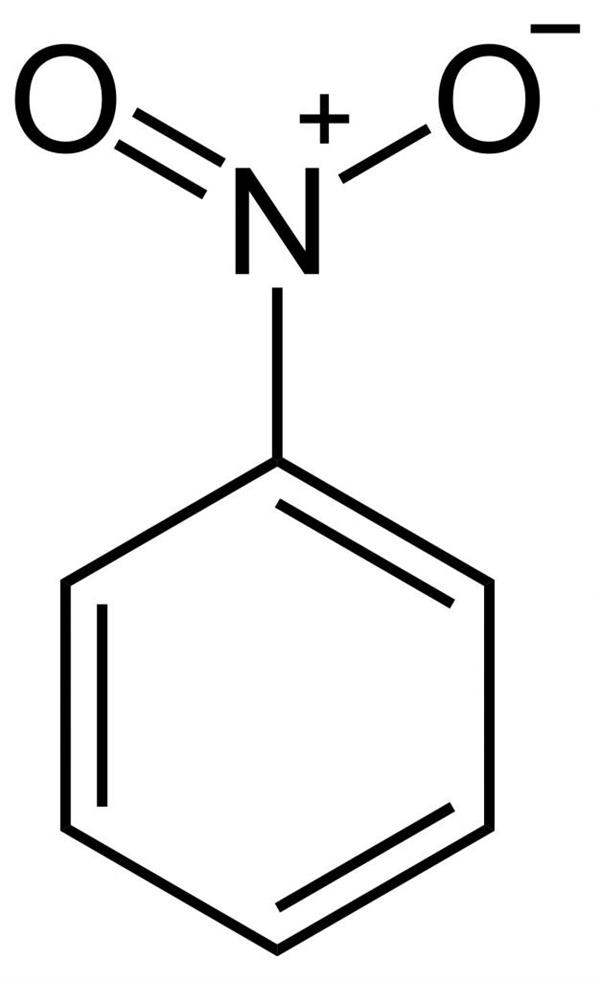
Структурна формула нітробензолу
Нитрогруппа — це дуже сильний акцептором електронної щільності. Тому молекула нітробензолу володіє негативним індуктивним і негативним мезомерным ефектом. Нитрогруппа досить сильно притягує на себе електронну густину ароматичного ядра, дезактівіруя його. Электрофильные реагенти вже не так сильно притягуються до ядра, і тому нітробензол не так активно набирає подібні реакції. Щоб приєднати безпосередньо до нитробензолу ще одну нітрогрупу, потрібні дуже жорсткі умови, набагато більш жорсткі, ніж при синтезі мононітробензола. Теж саме стосується галогенів, сульфогрупи та ін.
З структурної формули нітробензолу видно, що одна зв’язок азоту з киснем одинарна, а інша — подвійна. Але насправді, з-за мезомерного ефекту, вони обидві рівнозначні і мають однакову довжину 0,123 нм.