Візьміть в руки засіб для зняття лаку (здається, це речовина є у кожного в будинку або, як мінімум, хоч раз потрапляло на очі). На більшості з них в даний час видніється яскравий напис: без ацетону. Але далеко не всім відомо хоч що-небудь, крім назви, про хімічну речовину під назвою ацетон.
Що ж таке ацетон?
Хімічна формула ацетону гранично проста: C3H6O. Якщо чоловік був уважний на уроках хімії, то, можливо, він навіть пам’ятає клас хімічних сполук, до якого належить дана речовина, а саме – кетон. Або ж уважний в минулому учень школи може пам’ятати не тільки хім. формулу ацетону і клас з’єднання, а ще й структурну формулу, яка представлена на малюнку нижче.
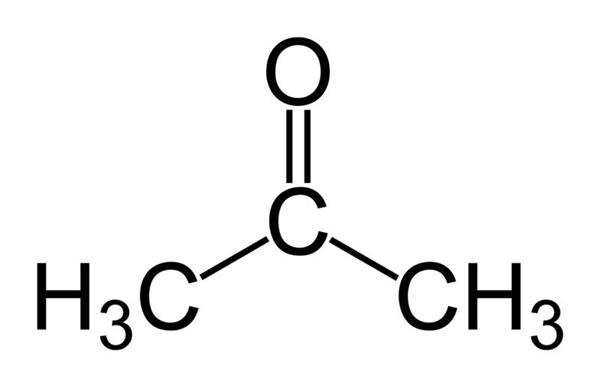
Крім структури, формула ацетону відображає і його загальноприйняте за номенклатурою ІЮПАК назва: пропанон-2. Хоча знову варто відзначити, що деякі читачі, можливо, навіть пам’ятають правила назви хімічних речовин зі шкільної лави.
А якщо говорити про те, що криється під формулою ацетону в реальному житті, а не на картинці з формулою або структурою? Ацетон при нормальних умовах являє собою летку рідину без кольору, але з характерним різким запахом. Можна бути точно впевненим в тому, що з запахом ацетону знайомий майже кожен чоловік.

