Біфторид амонію — токсична неорганічне з’єднання промислового виробництва, що використовується в скляній, нафтової й металургійної сферах. Речовина часто застосовується в якості заміни плавикової кислоти або фтористого водню.
Загальний опис та фізичні властивості
Біфторид амонію найчастіше має твердий агрегатний стан і представлено у вигляді кристалів. Останні характеризуються високою розчинністю у воді, але нульовий — в ацетоні і спирті. Кристали мають орторомбическую сингонию з дискретною групою рухів Р man. Речовина розкладається при температурі понад 238 °С.

Даний біфторид не має пожежонебезпечними та вибухонебезпечними властивостями.
Структура і хімічна формула
Речовина має декілька синонімічних найменувань, таких як біфторид фториду амонію, амоній фтористий кислий, гидрофторид амонію і т. д. Це з’єднання має хімічну формулу NH4(HF2).
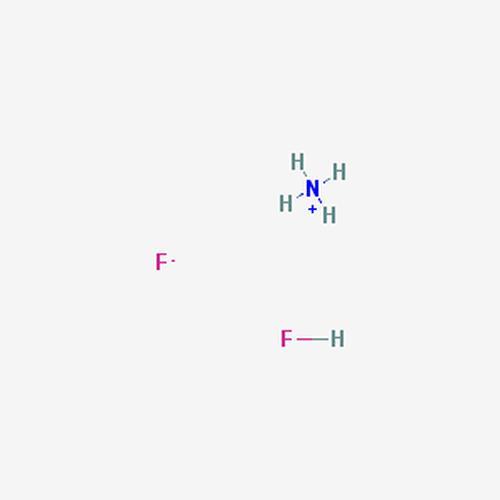
В хімічний склад речовини входять:
- катіон амонію (NH4+);
- біфторид або водень діфторіда;
- аніон (HF2-).
Примітною особливістю цього з’єднання є присутність найсильнішою водневої зв’язку з довжиною 114 мкм. Вона з’єднує фтор і водень в центросимметричном триатомном бифторидном анионе. Енергія зв’язку перевищує 155 кДж/моль-1.
В кристалічній формі речовини кожен катіон амонію оточують чотири фторідних центру, утворюючи тетраедр.

