Лінійчаті спектри – це, мабуть, одна з важливих тем, які розглядаються в курсі фізики 8 класу в розділі оптики. Важлива вона тому, що дозволяє зрозуміти атомну будову, а також використовувати ці знання для вивчення нашої Всесвіту. Розглянемо в статті це питання.
Поняття про електромагнітних спектрах
В першу чергу пояснимо, про що піде мова в статті. Кожен знає, що видимий нами сонячне світло являє собою електромагнітні хвилі. Будь-яка хвиля характеризується двома важливими параметрами – це її довжина і частота (третім не менш важливим її властивістю є амплітуда, що відображає інтенсивність випромінювання).
У разі електромагнітного випромінювання обидва параметра пов’язані наступне рівність: λ*ν = c, де грецькими літерами λ (лямбда) і ν (ню) зазвичай позначають довжину хвилі і її частоту, відповідно, а c – швидкість світла. Оскільки остання є величиною постійною для вакууму, то довжина і частота електромагнітних хвиль обернено пропорційні один одному.
Електромагнітним спектром у фізиці прийнято називати сукупність різних довжин хвиль (частот), які випускаються відповідним джерелом випромінювання. Якщо ж речовина поглинає, а не випромінює хвилі, тоді говорять про спектрі адсорбції або поглинання.
Які бувають електромагнітні спектри?
У загальному випадку існує два критерії їх класифікації:
- По частоті випромінювання.
- За способом розподілу частот.
Не будемо в цій статті зупинятися на розгляді 1-го типу класифікації. Тут лише коротко скажемо, що існують електромагнітні хвилі високих частот, які називаються гамма-випромінюванням (>1020 Гц) і рентгенівським (1018-1019 Гц). Ультрафіолетовий спектр являє собою вже менші частоти (1015-1017 Гц). Видимий або оптичний спектр лежить в області частот 1014 Гц, що відповідає набору довжин від 400 до 700 мкм мкм (деякі люди здатні бачити трохи “ширше”: від 380 мкм до 780 мкм). Більш низькі частоти відповідають інфрачервоного, або теплового спектру, а також радіохвилях, які вже в довжину можуть досягати кількох кілометрів.
Далі в статті докладно розглянемо 2-й тип класифікації, який відзначений у списку вище.
Лінійчаті і безперервні спектри випромінювання
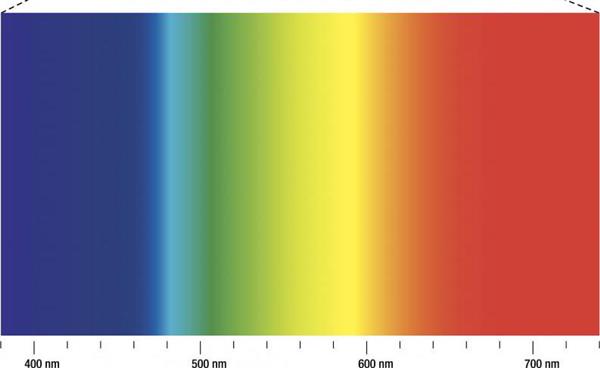
Абсолютно будь-яка речовина, якщо його нагріти, почне випромінювати електромагнітні хвилі. Будь частот і довжин хвиль вони будуть? Відповідь на це питання залежить від того, в якому агрегатному стані знаходиться досліджувана речовина.
Рідкі і тверді тіла випромінюють, як правило, безперервний набір частот, тобто різниця між ними настільки невелика, що можна вести мову про безперервному спектрі випромінювання. У свою чергу, якщо атомарний газ, має невисокі тиску, нагріти, то він почне “світитися”, випускаючи строго певні довжини хвиль. Якщо останні проявити на фотоплівці, то вони будуть представляти собою вузькі лінії, кожна з яких відповідає за конкретну частоту (довжину хвилі). Тому цей вид випромінювання був названий лінійчатим спектром випромінювання.
Між лінійчатим і безперервним існує проміжний тип спектру, який випромінює зазвичай молекулярний, а не атомарний газ. Цей тип являє собою ізольовані смуги, кожна з яких, при її детальному розгляді, складається з окремих вузьких ліній.
Лінійчатий спектр поглинання
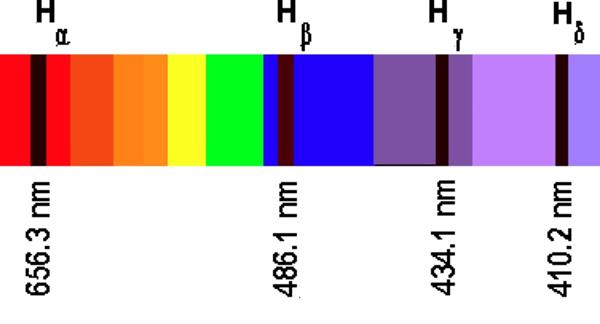
Все сказане в попередньому пункті відносилося до випромінювання хвиль з речовиною. Але воно також має поглинальною здатністю. Проведемо звичайний експеримент: візьмемо холодний розряджений атомарний газ (наприклад, аргон або неон) і пропустимо через нього білий світло від лампи розжарювання. Після цього проаналізуємо пройшов через газ світловий потік. Виявиться, що якщо розкласти цей потік на окремі частоти (це можна зробити за допомогою призми), то в спостережуваному безперервному спектрі з’являться чорні смуги, які свідчать, що ці частоти були поглинені газом. У цьому випадку говорять про линейчатом спектрі поглинання.
У середині XIX ст. німецький вчений по імені Густав Кірхгоф відкрив дуже цікаву властивість: він зауважив, що місця, в яких на суцільному спектрі з’являються чорні лінії, точно відповідають частотам випромінювання даної речовини. В даний час названа особливість носить назву закону Кірхгофа.
Серії Бальмера, Лиману і Пашена
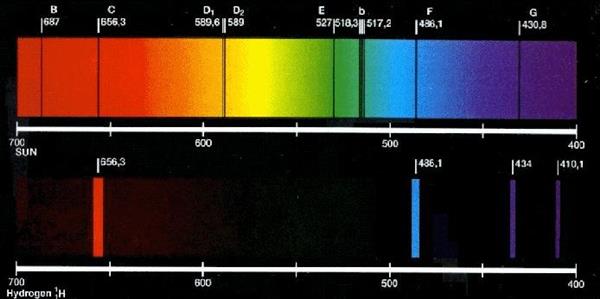
З кінця XIX століття фізики усього світу прагнули зрозуміти, що являють собою лінійчаті спектри випромінювання. Було встановлено, що кожен атом даного хімічного елемента при будь-яких умовах проявляє однакову випромінювальну здатність, тобто випромінює електромагнітні хвилі тільки конкретних частот.
Перші детальні дослідження цього питання були проведені швейцарським фізиком Бальмер. У своїх експериментах він використовував водневий газ, розігрітий до високих температур. Оскільки атом водню є найпростішим серед всіх відомих хімічних елементів, то на ньому найпростіше проводити вивчення особливостей спектру випромінювання. Бальмер отримав дивовижний результат, який він записав у вигляді наступної формули:
1/λ=RH*(1/4-1/n2).
Тут λ – довжина випромінюваної хвилі, RH – деяка постійна величина, яка для водню дорівнює 1,097*107 м-1, n – ціле число, починаючи з 3-х, тобто 3, 4, 5 і т. д.
Всі довжини λ, які виходять з цієї формули, лежать в межах оптичного спектра видимого людиною. Ця серія значень λ для водню отримала назву спектру Бальмера.
Згодом, використовуючи відповідне обладнання, американський вчений Теодор Лиман відкрив ультрафіолетовий водневий спектр, який він описав формулою, подібною бальмеровской:
1/λ=RH*(1/1-1/n2).
Нарешті, ще один німецький фізик, Фрідріх Ріллі, отримав формулу для випромінювання водню в інфрачервоній області:
1/λ=RH*(1/9-1/n2).
Тим не менш тільки розвиток квантової механіки в 20-ті роки XX століття змогло дати пояснення цим формулам.
Резерфорд, Бор і атомна модель

У перше десятиліття XX століття Ернест Резерфорд (британський фізик новозеландського походження) провів багато експериментів з вивчення радіоактивності різних хімічних елементів. Завдяки цим дослідженням народилася перша модель атома. Резерфорд вважав, що ця “крупинка” матерії складається з ядра електрично позитивного і обертових за його орбітами електронів і негативних. Кулонівські сили пояснюють, чому атом “не розвалюється”, а відцентрові сили, що діють на електрони, є причиною, чому останні не падають на ядро.
Все, здавалося б, логічно в цій моделі, за винятком одного “але”. Справа в тому, що при русі по криволінійній траєкторії будь-яка заряджена частинка повинна випромінювати електромагнітні хвилі. Але у випадку стабільного атома цього ефекту не спостерігається. Тоді виходить, що невірна сама модель?
Необхідні поправки до неї вніс інший фізик – датчанин Нільс Бор. Ці поправки в даний час відомі як його постулати. Бор ввів два положення в модель Резерфорда:
- електрони рухаються по стаціонарних орбітах в атомі, при цьому вони не випромінюють і не поглинають фотони;
- процес випромінювання (поглинання) відбувається тільки тоді, коли електрон переходить з однієї орбіти на іншу.
Що являють собою стаціонарні боровские орбіти, розглянемо у наступному пункті.
Квантованность енергетичних рівнів
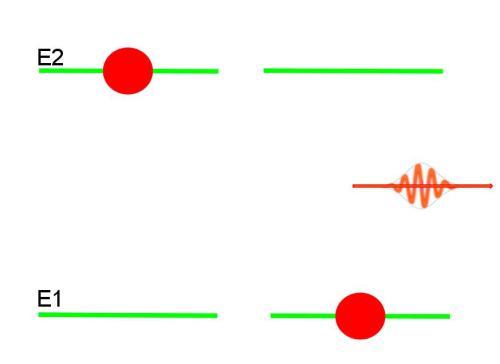
Стаціонарні орбіти електрона в атомі, про яких вперше заговорив Бор, є стабільними квантовими станами цієї частки-хвилі. Ці стани характеризуються певною енергією. Останнє означає, що електрон в атомі знаходиться в деякій енергетичної “ямі”. Потрапити в іншу “яму” він може, якщо отримає додаткову енергію ззовні у вигляді фотона.
У лінійчатих спектрів поглинання і флуоресценції для водню, формули яких наведено вище, можна побачити, що перший член в дужках являє собою деяке число виду 1/m2, де m=1, 2, 3.. – ціле число. Воно відображає номер стаціонарної орбіти, на яку переходить електрон з більш високого енергетичного рівня n.
Як вивчають спектри у видимому діапазоні?

Вище вже було сказано, що для цього використовують скляні призми. Вперше це зробив Ісаак Ньютон в 1666 році, коли розклав видиме світло на набір кольорів веселки. Причина, по якій спостерігається цей ефект, що полягає в залежності коефіцієнта заломлення від довжини хвилі. Так, синій колір (короткі хвилі) переломлюється сильніше, ніж червоний (довгі хвилі).
Відзначимо, що в загальному випадку при русі пучка електромагнітних хвиль в якій-небудь матеріальній середовищі високочастотні складові цього пучка завжди переломлюються і розсіюються сильніше, ніж низькочастотні. Яскравим прикладом є блакитний колір неба.
Оптика лінзи і видимий спектр
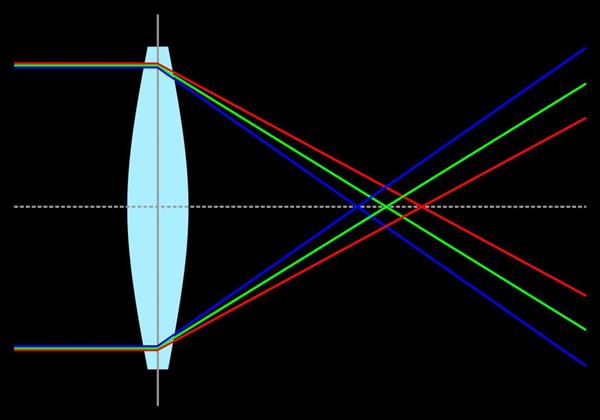
При роботі з лінзами часто використовується сонячне світло. Оскільки він являє собою безперервний спектр, то при проходженні через лінзу його частоти переломлюються по-різному. У підсумку оптичний прилад виявляється нездатним зібрати весь світло в одну точку, і з’являються райдужні відтінки. Цей ефект відомий під назвою хроматична аберація.
Зазначена проблема оптики лінзи частково вирішується за допомогою комбінації оптичних стекол у відповідних приладах (мікроскопах, телескопах).

