Парціальний тиск
Закон Дальтона для суміші ідеальних газів передбачає знання ще про одному макроскопічному параметрі – парціальному тиску.
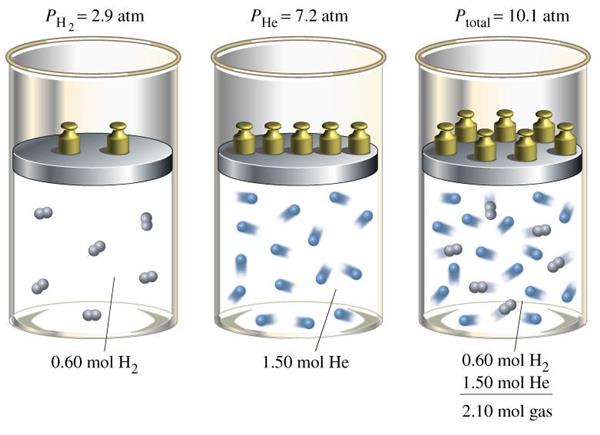
Припустимо, що є деяка суміш, що складається з 2-х компонентів, наприклад, H2 і He. Ця суміш знаходиться в посудині конкретного обсягу і на його стінки створює певний тиск. Оскільки молекули водню і атоми гелію не взаємодіють один з одним, тоді для будь-яких розрахунків макроскопічних характеристик обидва компоненти можна розглядати незалежно один від одного.
Парціальним тиском компонента називається тиск, що він створює незалежно від інших компонентів суміші, займаючи наданий йому об’єм. У розглянутому прикладі можна говорити про парціальному тиску H2 і такої ж характеристики для He. Ця величина виражається в паскалях і позначається для i-го компонента як Pi.

