Хімічні властивості
Для альдегідів характерні такі типи реакцій:
- за приєднання карбонільної групи;
- полімеризації;
- конденсації;
- відновлення і окиснення.
Більшість реакцій йде за механізмом нуклеофільного приєднання по зв’язку С=О.
Зазвичай розглядають хімічні властивості альдегідів на прикладі оцтового альдегіду.
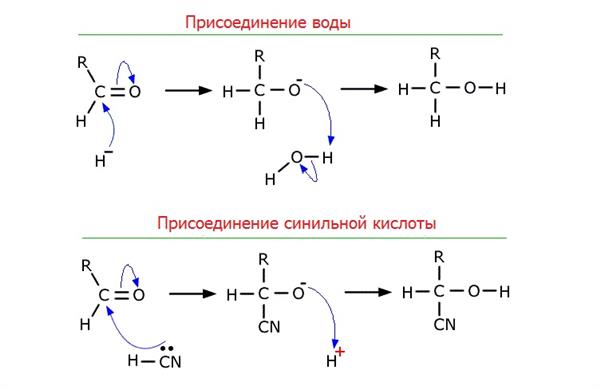
Реакції приєднання
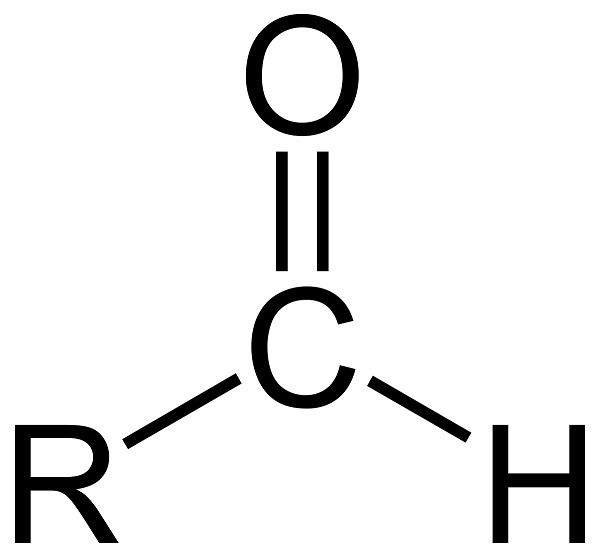
У карбонільної групи С=О електронна щільність зміщена до атома кисню, тому на карбонильном атомі вуглецю формується частковий позитивний заряд, який обумовлює хімічну активність альдегідів. Позитивний заряд на атомі вуглецю групи С=забезпечує його активність в реакціях з нуклеофільними реагентами – водою, спиртом, магній органічними сполуками. Атом кисню води може атакувати карбонильный атом вуглецю, приєднуватися до нього і викликати розрив зв’язку С=О.
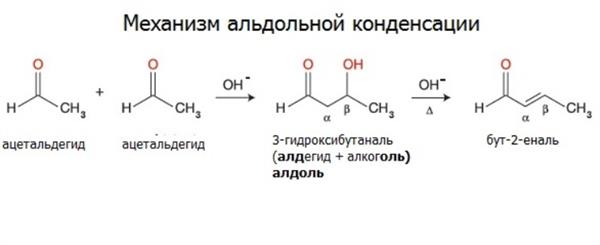
Реакції конденсації
Альдегіди вступають у реакції альдольної і кротоновой конденсації.
Ацетальдегід при дії слабкого розчину лугу на холоду перетворюється в альдоль. Продуктом реакції є рідина, змішується з водою при зниженому тиску. Це речовина містить як альдегидную, так і спиртову групу (звідси і назва).